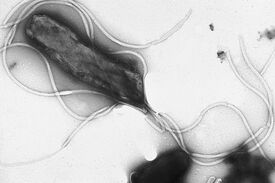
| Helicobacter pylori | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Научная классификация | |||||||||||||||
|
|||||||||||||||
| Латинское название | |||||||||||||||
| Helicobacter pylori (Marshall et al. 1985) Goodwin et al. 1989 | |||||||||||||||
|
Helicobacter pylori (хе́ликоба́ктер пило́ри, более правильная транскрипция — ге́ликоба́ктер пило́ри[1]) — спиралевидная грамотрицательная бактерия, которая инфицирует различные области желудка и двенадцатиперстной кишки. Многие случаи язв желудка и двенадцатиперстной кишки, гастритов, дуоденитов, и, возможно, некоторые случаи лимфом желудка и рака желудка этиологически связаны с инфицированием Helicobacter pylori. Однако у многих инфицированных носителей Helicobacter pylori не обнаруживается никаких симптомов заболевания.
Спиралеобразная форма бактерии, от которой, собственно, и произошло родовое название Helicobacter, как полагают, связана с приобретением этим микроорганизмом в ходе эволюции способности проникать в слизистую оболочку желудка и двенадцатиперстной кишки, и с тем, что такая форма облегчает её движение в слизистом геле, покрывающем слизистую оболочку желудка.[2]
История открытия[]
В 1875 году немецкие учёные обнаружили спиралевидную бактерию в слизистой оболочке желудка человека. Эта бактерия не росла в культуре (на известных в то время искусственных питательных средах), и это случайное открытие было в конце концов забыто.[3]
В 1893 году итальянский исследователь Джулио Биззоцеро описал похожую спиралевидную бактерию, живущую в кислом содержимом желудка собак.[4]
В 1899 году польский профессор Валерий Яворский из Ягеллонского университета в Кракове, исследуя осадок из промывных вод желудка человека, обнаружил, помимо бактерий, напоминавших по форме хворостины, также некоторое количество бактерий характерной спиралеобразной формы. Он назвал обнаруженную им бактерию Vibrio rugula. Он был первым, кто предположил возможную этиологическую роль этого микроорганизма в патогенезе заболеваний желудка. Его работа на эту тему была включена в польское «Руководство по заболеваниям желудка». Однако эта работа не имела большого влияния на остальной врачебный и научный мир, поскольку была написана на польском языке.[5]
Бактерия была вновь открыта в 1979 году австралийским патологом Робином Уорреном, который затем провёл дальнейшие исследования её вместе с Барри Маршаллом, начиная с 1981 года. Уоррену и Маршаллу удалось выделить и изолировать этот микроорганизм из проб слизистой оболочки желудка человека. Они также были первыми, кому удалось культивировать этот микроорганизм на искусственных питательных средах.[6] В оригинальной публикации[7] Уоррен и Маршалл высказали предположение, что большинство язв желудка и гастритов у человека вызываются инфицированием микроорганизмом Helicobacter pylori, а не стрессом или острой пищей, как предполагалось ранее.[8]

Гистологический препарат слизистой желудка, демонстрирующий хеликобактерный гастрит и колонизацию слизистой хеликобактером. Окраска серебром по Warthin-Starry.
Медицинское и научное сообщество медленно и неохотно признавали патогенетическую роль этой бактерии в развитии язв желудка и двенадцатиперстной кишки и гастритов, вследствие распространённого в то время убеждения, что никакой микроорганизм не в состоянии выжить сколько-нибудь длительное время в кислом содержимом желудка. Признание научным сообществом этиологической роли этого микроба в развитии заболеваний желудка начало постепенно приходить лишь после того, как были проведены дополнительные исследования. Один из наиболее убедительных экспериментов в этой области был поставлен Барри Маршаллом: он сознательно выпил содержимое чашки Петри с культурой бактерии H. pylori, после чего у него развился гастрит.[9] Бактерия была обнаружена в слизистой его желудка, тем самым были выполнены три из четырёх постулатов Коха. Четвёртый постулат был выполнен, когда на второй эндоскопии, спустя 10 дней после преднамеренного заражения, были обнаружены признаки гастрита и присутствие H. pylori. Затем Маршалл сумел продемонстрировать, что он в состоянии излечить свой хеликобактерный гастрит с помощью 14-дневного курса лечения солями висмута и метронидазолом.[9] Маршалл и Уоррен затем пошли дальше и сумели показать, что антибиотики эффективны в лечении многих, если не большинства, случаев гастрита и язв желудка и двенадцатиперстной кишки.[9]
В 1994 году Американский Национальный Институт Здравоохранения опубликовал экспертное мнение, в котором утверждалось, что большинство рецидивирующих язв желудка и гастритов с повышенной кислотностью вызываются инфицированием микробом H. pylori, и рекомендовал включать антибиотики в терапевтические режимы при лечении язвенной болезни желудка, а также гастритов с повышенной кислотностью.[10] Постепенно накапливались данные также о том, что язвы двенадцатиперстной кишки и дуодениты также ассоциированы с инфицированием H. pylori.[11][12]
В 2005 году первооткрыватели медицинского значения бактерии Робин Уоррен и Барри Маршалл были удостоены Нобелевской премии по медицине.[13]
До того, как стала понятна роль инфекции Helicobacter pylori в развитии язвенной болезни желудка и двенадцатиперстной кишки и гастритов, язвы и гастриты обычно лечили лекарствами, которые нейтрализуют кислоту (антациды) или снижают её продукцию в желудке (ингибиторы протонного насоса, блокаторы H2-гистаминовых рецепторов, М-холинолитики и др.). Хотя такое лечение в ряде случаев бывало эффективным, язвы и гастриты весьма часто рецидивировали после прекращения лечения. Весьма часто используемым препаратом для лечения гастритов и язвенной болезни желудка и двенадцатиперстной кишки был висмута субсалицилат (пепто-бисмол). Он часто был эффективен, но вышел из употребления, поскольку его механизм действия оставался непонятным. Сегодня стало понятно, что эффект пепто-бисмола был обусловлен тем, что соли висмута действуют на Helicobacter pylori как антибиотик. На сегодняшний день большинство случаев язв желудка и двенадцатиперстной кишки, гастритов и дуоденитов с доказанной лабораторными тестами хеликобактерной этиологией, особенно в развитых странах, лечат антибиотиками, эффективными против Helicobacter pylori.[14]
Хотя H. pylori остаётся наиболее медицински значимой бактерией, способной обитать в желудке человека, у других млекопитающих и некоторых птиц были найдены другие представители рода Helicobacter. Некоторые из них способны заражать и человека. Виды рода Helicobacter были также обнаружены в печени некоторых млекопитающих, причём они способны вызывать поражения и заболевания печени.[15]
Систематика[]
Бактерия была вначале названа Campylobacter pyloridis в 1985 году, затем название было исправлено в соответствии с правилами латинской грамматики на Campylobacter pylori в 1987 году[16], и только в 1989 году, после того, как анализ последовательностей ДНК этой бактерии показал, что в действительности она не принадлежит к роду Campylobacter, её и близкие ей виды выделили в отдельный род, Helicobacter Goodwin et al. 1989.[17] Название pylōri происходит от «pylorus» (привратник желудка, циркулярный жом, перекрывающий проход из желудка в двенадцатиперстную кишку), которое, в свою очередь, происходит от греческого слова πυλωρός, означающего буквально «привратник».
Многие виды рода Helicobacter являются патогенными для человека и животных и обитают в ротовой полости, желудке, различных отделов кишечника человека и животных (патогенными для человека и животных кроме H. pylori являются также виды H. nemestrinae, H. acinonychis, H. felis, H. bizzozeronii и H. salomonis)).[18] Наибольший уровень сходства по результатом ДНК-ДНК гибридизации отмечен между видами H. pylori и H. mustelae.[18]
Виды рода Helicobacter являются единственными известными на сегодняшний день микроорганизмами, способными длительно выживать в чрезвычайно кислом содержимом желудка и даже колонизировать его слизистую.[19]
Разработано много методов определения как внутривидовой дифференциации штамов H. pylori, так и для дифференцировки от других видов рода Helicobacter, такие как биотипические, и серологические методы, методы определения уреазной активности и токсинообразования, так и молекулярные — белковый электрофорез клеточного лизата, метод определения полиморфизма длин рестрикционных фрагментов (ПДРФ), полимеразная цепная реакция (ПЦР), секвенирование 16S рибосомальной РНК[18] Показан высокий уровень внутривидового полиморфизма штаммов H. pylori по сравнению с крайне близким видом H. mustelae, проявляющим высокий уровень консерватизма. Полиморфизм заключается в однонуклеотидных заменами, а также крупных внутригеномных перестройках, и высоких частотах трансформации.[18]
Типовые штаммы H. pylori: ATCC 43504, DSM 4867, JCM 7653, LMG 7539, NCTC 11637.[18]
Строение[]

Размеры и схематическое строение H. pylori
Helicobacter pylori — спиралевидная грамотрицательная бактерия, около 3 мкм в длину, диаметром около 0,5 мкм. Она обладает 4-6 жгутиками и способностью чрезвычайно быстро двигаться даже в густой слизи или агаре. Она микроаэрофильна, то есть требует для своего развития наличия кислорода, но в значительно меньших концентрациях, чем содержащиеся в атмосфере.
Бактерия содержит гидрогеназу, которая может использоваться для получения энергии путём окисления молекулярного водорода, продуцируемого другими кишечными бактериями.[20] Бактерия также вырабатывает оксидазу, каталазу и уреазу.
Helicobacter pylori обладает способностью формировать биоплёнки (англ.) , способствующие невосприимчивости бактерии к антибиотикотерапии и защищающие клетки бактерий от иммунного ответа хозяина.[21] Предполагают, что это увеличивает её выживаемость в кислой и агрессивной среде желудка.
В неблагоприятных условиях, а также в «зрелых» или старых культурах Helicobacter pylori обладает способностью превращаться из спиралевидной в круглую или шарообразную кокковидную форму. Это благоприятствует её выживанию и может являться важным фактором в эпидемиологии и распространении бактерии.[22] Кокковидная форма бактерии не поддаётся культивированию на искусственных питательных средах (хотя может спонтанно возникать по мере «старения» культур), но была обнаружена в водных источниках в США и других странах. Кокковидная форма бактерии также обладает способностью к адгезии к клеткам эпителия желудка in vitro.
Кокковидные клетки отличаются деталями строения клеточной стенки (преобладанием N-ацетил-D-глюкозаминил-β(1,4)-N-ацетилмурамил-L-Ала-D-Глю мотива в пептидогликане клеточной стенки (GM-дипептида)), изменение строения клеточной стенки приводит к неузнаванию бактерии иммунной системой хозяина (бактериальная мимикрия).[23]
Геном[]
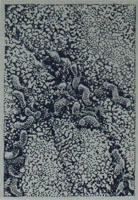
Электронно-микроскопическая фотография H. pylori
Известно несколько штаммов Helicobacter pylori, и геном трех из них полностью секвенирован.[24][25][26][27]
Геном штамма «26695» и геном штамма «J99» демонстрируют значительные генетические различия, до 6 % нуклеотидов у них различны.
Изучение генома H. pylori ведётся в основном с целью улучшить наше понимание патогенеза гастритов и язвенной болезни желудка, причин способности этого микроорганизма вызывать заболевание. На данный момент в базе данных генома Helicobacter pylori 62 гена отнесены к категории «генов патогенных» (то есть их наличие у бактерии коррелирует с её патогенностью). Оба изученных штамма имеют общий «остров патогенности» (общую последовательность генов, имеющих отношение к вирулентности и патогенности хеликобактера) длиной около 40 Кб, так называемый Cag. Этот участок содержит более 40 генов. Он обычно отсутствует у штаммов, которые выделены от людей, являющихся бессимптомными носителями H. pylori.
Ген cagA кодирует один из важнейших белков вирулентности H. pylori. Штаммы, имеющие ген cagA ассоциированны со способностью вызывать тяжёлые формы язвы желудка. Ген cagA кодирует белок длинной 1186 аминокислотных остатка. Белок cagA транспортируется внутрь клеток, где он нарушает нормальное функционирование цитоскелета. Остров патогенности Cag состоит из примерно 30 генов, кодирующих сложную систему секреции типа IV.[28]. После адгезии H.pylori к клеткам эпителия желудка, cagA впрыскивается в клетку посредством системы секреции типа IV. Белок cagA фосфолирируется тирозиновыми протеинкиназами клетки и взаимодействует с фосфатазой Src, изменяя морфологию клеток.[29] Вирулентные штаммы H. pylori способны активировать рецептор эпидермального фактора роста (epidermal growth factor receptor, EGFR), мембранный белок с тирозинкиназным доменом. Активация EGFR H. pylori ассоциирована с изменённой сигнальной трансдукцией и изменением профиля экспрессии генов клетки хозяина, что может влиять на течение патологического процесса.[30]
Показана синергетичность действия генов babA2, cagA, и s1 vacA при патологическом процессе, вовлечённом в метаплазии кишечника.[31] Продукты генов cagA и babA2 идентифицируются иммуногистохимически, гистологически и при помощи in situ гибридизации при метаплазии кишечника и злокачественных новообразованиях желудка, ассоциированных с хеликобактерной инфекцией и могут служить возможными диагностическими маркерами.[32]
Также идентифицированы некоторые гены, ассоциированные со способностью к колонизации эпителия желудка, такие как flg, flh, tlp (отвечают за наличие жгутиков и хемотаксис), ureA, nixA, amiE (гены, отвечающие за синтез уреазы и продукцию аммиака), fur, pfr, fecA, frpB (гены, отвечающие за метаболизм железа), sod, hptG (ответ на стресс), и algA, rfaJ, lpxB (гены, отвечающие за биосинтез липополисахарида и экзополисахарида).[33] Показана роль в реакциях Helicobacter pylori на внешние раздражители продукта гена tlpD, предположительно кодирующего сенсорный белок.[34]
Факторы вирулентности[]

Факторы вирулентности геликобактера
Способность H. pylori колонизировать слизистую желудка и вызывать гастрит либо язву желудка зависит не только от состояния иммунитета организма хозяина, но и от индивидуальных особенностей конкретного штамма бактерии.[35]
Одним из важных факторов вирулентности хеликобактер является наличие у неё жгутиков, благодаря которым обеспечивается быстрое движение микроорганизма в слое густой слизи, защищающей слизистую желудка от воздействия кислоты, её хемотаксис в места скопления других бактерий этого вида и быстрая колонизация слизистой.
Липополисахариды и белки наружной оболочки бактерии обладают свойством адгезии к наружной оболочке мембран клеток слизистой желудка. Кроме того, липополисахариды наружной оболочки H. pylori вызывают иммунный ответ организма хозяина и развитие воспаления слизистой.
Секретируемые бактерией во внешнюю среду литические ферменты — муциназа, протеаза, липаза — вызывают деполимеризацию и растворение защитной слизи (состоящей в основном из муцина) и повреждение слизистой желудка.

Молекулярная модель уреазы H. pylori
Очень важную роль в вирулентности бактерии и в её способности выживать в кислом содержимом желудка играет секреция бактерией уреазы — фермента, расщепляющего мочевину с образованием аммиака. Аммиак нейтрализует соляную кислоту желудка и обеспечивает бактерии локальное поддержание комфортного для неё pH (около 6-7).
Продукция хеликобактером различных экзотоксинов, в частности, вакуолизирующего экзотоксина (продукта гена vacA), также вызывает вакуолизацию, повреждение и гибель клеток слизистой желудка.
Специальная «инжекционная система», имеющаяся у хеликобактер, предназначена для непосредственного впрыскивания в клетки слизистой оболочки желудка различных эффекторных белков (в частности, продуктов гена cagA), вызывающих воспаление, повышение продукции интерлейкина-8[36], угнетение апоптоза и избыточный рост определённых типов клеток. Полагают, что именно этим обусловлена наблюдающаяся при геликобактерной инфекции гиперплазия париетальных (кислотообразующих) клеток желудка, гиперсекреция соляной кислоты и пепсина, и в конечном итоге повышение вероятности рака желудка.[37]
Штаммы H. pylori, выделенные от больных с язвой желудка или двенадцатиперстной кишки, как правило, проявляют большую биохимическую агрессивность, чем штаммы, выделенные от больных с гастритом, а штаммы, выделенные от больных с гастритом, обычно более агрессивны и вирулентны, чем штаммы, выделенные от бессимптомных носителей.[35] В частности, штаммы, выделенные от больных с язвенной болезнью, чаще бывают cagA-положительными (то есть продуцирующими cagA эффекторные белки). Штаммы, выделенные от больных с гастритом, чаще продуцируют экзотоксин vacA, чем штаммы, выделенные от бессимптомных носителей.[38][39]
Патогенетические механизмы[]

Схематическое изображение патогенеза язвы желудка
На начальном этапе после попадания в желудок H. pylori, быстро двигаясь при помощи жгутиков, преодолевает защитный слой слизи и колонизирует слизистую оболочку желудка. Закрепившись на поверхности слизистой, бактерия начинает вырабатывать уреазу, благодаря чему в слизистой оболочке и слое защитной слизи поблизости от растущей колонии растёт концентрация аммиака и повышается pH. По механизму отрицательной обратной связи это вызывает повышение секреции гастрина клетками слизистой желудка и компенсаторное повышение секреции соляной кислоты и пепсина, с одновременным снижением секреции бикарбонатов.
Муциназа, протеаза и липаза, вырабатываемые бактерией, вызывают деполимеризацию и растворение защитной слизи желудка, в результате чего соляная кислота и пепсин получают непосредственный доступ к оголённой слизистой желудка и начинают её разъедать, вызывая химический ожог, воспаление и изъязвление слизистой оболочки.
Экзотоксин VacA, вырабатываемый бактерией, вызывают вакуолизацию и гибель клеток эпителия желудка.[40] Продукты гена cagA вызывают дегенерацию клеток эпителия желудка, вызывая изменения фенотипа клеток (клетки становятся удлинёнными, приобретая так называемый «колибри фенотип»[41]). Привлечённые воспалением (в частности, секрецией интерлейкина-8 клетками слизистой желудка) лейкоциты вырабатывают различные медиаторы воспаления, что приводит к прогрессированию воспаления и изъязвления слизистой, бактерия также вызывает окислительный стресс и запускает механизм программируемой клеточной смерти клеток эпителия желудка.[42]
Диагностика инфекции[]

Иммуногистохимическая окраска H. pylori в биоптате слизистой желудка.
Диагностика геликобактерной инфекции обычно производится путём опроса больного на наличие диспептических жалоб и симптомов, и затем выполнения тестов, которые могут помочь подтвердить или опровергнуть факт наличия хеликобактерной инфекции.
Неинвазивные (не требующие эндоскопии) тесты на наличие хеликобактерной инфекции включают в себя определение титра антител в крови к антигенам H. pylori, определение наличия антигенов H. pylori в кале, а также уреазный дыхательный тест, состоящий в том, что пациент выпивает раствор меченой 14C- или 13C-углеродом мочевины, которую бактерия расщепляет с образованием меченой, соответственно, 14C- или 13C- двуокиси углерода, которая затем может быть обнаружена в выдыхаемом воздухе при помощи масс-спектрометрии.
Существуют также уреазные дыхательные тесты, основанные на определении концентрации аммиака в выдыхаемом воздухе.[43] Данные методы предполагают приём пациентом мочевины нормального изотопного состава и последующее измерение концентрации аммиака с помощью газоанализатора. К достоинствам метода можно отнести невысокую стоимость обследования, скорость получения результатов, высокую чувствительность (96 %), значительно меньшую стоимость оборудования по сравнению с масс-спектрографами.
Однако самым надёжным и «референсным» методом диагностики хеликобактерной инфекции остаётся биопсия, производимая во время эндоскопического обследования желудка и двенадцатиперстной кишки. Взятую при биопсии ткань слизистой подвергают быстрому тестированию на наличие уреазы и антигенов геликобактера, гистологическому исследованию, а также культуральному исследованию с выделением хеликобактера на искусственных питательных средах.
Ни один из методов диагностики хеликобактерной инфекции не является полностью достоверным и защищённым от диагностических ошибок и неудач. В частности, результативность биопсии в диагностике хеликобактерной инфекции зависит от места взятия биоптата, поэтому при эндоскопическом исследовании обязательно взятие биоптатов из разных мест слизистой желудка. Тесты на наличие антител к антигенам хеликобактера имеют чувствительность всего лишь от 76 % до 84 %. Некоторые лекарства могут повлиять на активность уреазы, продуцируемой хеликобактером, в результате чего при исследовании уреазной активности при помощи меченой мочевины могут получиться ложноотрицательные результаты.
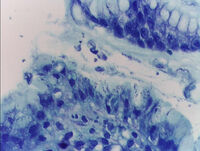
H. pylori в слизистой желудка. Окраска по Романовскому-Гимзе.
Хеликобактерная инфекция может сопровождаться симптомами или протекать бессимптомно (без каких-либо жалоб со стороны инфицированного). Предполагается, что до 70 % случаев хеликобактерной инфекции протекают бессимптомно и что около 2/3 человеческой популяции в мировом масштабе инфицированы геликобактером, что делает геликобактерную инфекцию самой распространённой инфекцией в мире. Истинная частота встречаемости бессимптомного носительства хеликобактера варьирует от страны к стране. В развитых странах Запада (Западная Европа, США, Австралия) эта частота составляет примерно 25 %, и значительно выше в странах так называемого «третьего мира», а также в посткоммунистических странах Восточной Европы и в особенности в странах бывшего Советского Союза. В странах третьего мира и в посткоммунистических странах, вследствие сравнительно низких санитарных стандартов и условий, не редкостью является обнаружение геликобактерной инфекции у детей и подростков. В Соединённых Штатах и Западной Европе хеликобактерная инфекция чаще всего встречается в старших возрастных категориях (около 50 % у лиц старше 60 лет, по сравнению с 20 % у лиц моложе 40 лет) и в наиболее бедных социально-экономических слоях.
Разница в частоте встречаемости хеликобактерной инфекции в развитых странах Запада и в странах «третьего мира» приписывается более строгому соблюдению гигиенических стандартов и широкому использованию антибиотиков. Однако со временем стала проявляться проблема антибиотикоустойчивости H. pylori.[44] В настоящее время многие штаммы хеликобактера в Европе, США и даже в развивающихся странах, уже устойчивы к метронидазолу.
Хеликобактер был выделен из кала, слюны и зубного налёта инфицированных пациентов, что объясняет возможные пути передачи инфекции — фекально-оральный или орально-оральный (например, при поцелуях, пользовании общей посудой, общими столовыми приборами, общей зубной щёткой или анилингусе). Возможно (и весьма часто встречается) заражение хеликобактером в учреждениях общественного питания. Иногда возможно заражение через инфицированные эндоскопы при проведении диагностической гастроскопии.

H. pylori в слизистой желудка. Окраска гематоксилин-эозином.
Считается, что в отсутствие лечения хеликобактерная инфекция, однажды колонизировав слизистую желудка, может существовать в течение всей жизни человека несмотря на иммуный ответ хозяина.[45][46] Однако у пожилых людей, а также у больных с давно существующим гастритом, хеликобактерная инфекция, вероятно, может самостоятельно исчезать, поскольку с возрастом или с давностью заболевания гастритом слизистая желудка становится всё более атрофичной, истончённой и менее пригодной для колонизации хеликобактером, менее благоприятной для обитания микроба. Вместе с тем, атрофический гастрит у пожилых, или гастрит, перешедший в стадию атрофического гастрита после многих лет болезни, поддаётся лечению гораздо труднее, чем хеликобактерные гастриты.
Процент острых хеликобактерных инфекций, которые переходят в хроническую персистирующую форму, точно не известен, однако в нескольких исследованиях, в которых изучалось естественное течение болезни без лечения в человеческих популяциях, сообщалось о возможности спонтанного самоизлечения (спонтанной элиминации микроба-возбудителя).[47][48]
Лечение Helicobacter pylori-ассоциированных заболеваний[]
У пациентов с язвой желудка, язвой двенадцатиперстной кишки и гастритом с доказанной хеликобактерной этиологией стандартным протоколом лечения является эрадикация Helicobacter pylori, то есть лечебный режим, направленный на полное уничтожение этого микроба в желудке с целью обеспечить условия для заживления язвы.
Стандартной терапией первой линии при хеликобактерной инфекции является на сегодняшний день так называемая «однонедельная трёхкомпонентная терапия». Австралийский гастроэнтеролог Томас Бороди ввёл первый известный режим «трёхкомпонентной терапии» (англ. triple therapy) в 1987 году.[49]
Сегодня стандартной «тройной терапией» является комбинация амоксициллина, кларитромицина и ингибитора протонного насоса, такого, как омепразол.[50]
За последние десятилетия были разработаны различные варианты «тройной терапии», в частности, использующие другие, более современные и мощные ингибиторы протонного насоса, такие, как эзомепразол, пантопразол, лансопразол, рабепразол, или использующие метронидазол вместо амоксициллина либо вместо кларитромицина у больных с аллергией к производным пенициллина или к макролидам.[51]
При отсутствии результатов трёхкомпонентной терапии в виде эрадикации H. pylori, назначается терапия второй линии. При отсутствии противопоказаний к применению препаратов висмута назначается так называемая «квадритерапия», включающая ингибиторы протонного насоса (рабепразол, эзомепразол, омепразол, лансопразол либо пантопразол), противоязвенные препараты и препараты для лечения гастроэзофагеального рефлюкса (препараты висмута), антибиотики (тетрациклин), а также метронидазол; в противном случае (при невозможности применения препаратов висмута) назначают трёхкомпонентную терапию, включающую ингибиторы протонного насоса.[52]
Отмечены случаи непродуктивности антибиотикотерапии хеликобактерной инфекции, связанные как с антибиотикорезистентностью, так и с наличием зон в желудочно-кишечном тракте, в которых бактерии защищены от действия антибиотиков.[53] Отмеченно появление полирезистентных к антибиотикам изолятов H. pylori[54], в том числе и кларитромицин-резистентных штаммов.[55] Также отмечены случаи появления хинолон-резистентных штаммов H. pylori.[56]
Также ведутся исследования по поиску и синтезу более эффективных и менее токсичных препаратов, направленных на эрадикацию H. pylori, показана эффективность in vitro препарата TG44[57], препарат NE-2001 в опытах in vitro проявлял высокую селективность по отношению к H. pylori[58] Показана эффективность пероральной вакцинации клеточным лизатом H. pylori на мышиной модели.[59]
Примечания[]
- ↑ Ходорковская Б. Б., Чернявский М. Н. Учебник латинского языка. — М.: «Медицина», 1964. — С. 15 — 18. — 351 с. — 38000 экз.
- ↑ Campylobacter and Helicobacter // Medical Microbiology / edited by Samuel Baron. — 4th edition. — Galveston: The University of Texas Medical Branch, 1996. — 1273 p. — ISBN 0-9631172-1-1
- ↑ Blaser MJ (2005). "An Endangered Species in the Stomach". Scientific American 292 (2): 38 — 45. PMID 15715390.
- ↑ Bizzozero, Giulio (1893). "Ueber die schlauchförmigen Drüsen des Magendarmkanals und die Beziehungen ihres Epitheles zu dem Oberflächenepithel der Schleimhaut". Archiv für mikroskopische Anatomie 42: 82 — 152.
- ↑ Konturek JW (2003 Dec). "Discovery By Jaworski Of Helicobacter pylori and its pathogenetic role in peptic ulcer, gastritis and gastric cancer". Journal of Physiology and Pharmacology 54 Suppl 3: 23 — 41. PMID 15075463.
- ↑ Professor Barry Marshall (англ.). YouTube (01.11.2007). Проверено 4 марта 2009.
- ↑ Marshall B. J. (1983). "Unidentified curved bacilli on gastric epithelium in active chronic gastritis.". Lancet 1 (8336): 1273 — 1275. PMID 6134060.
- ↑ Marshall B. J., Warren J. R. (1984). "Unidentified curved bacilli in the stomach of patients with gastritis and peptic ulceration.". Lancet 1 (8390): 1311 — 1315. PMID 6145023.
- ↑ 9,0 9,1 9,2 Barry J. Marshall Autobiography (англ.). Nobel Foundation (2005). Проверено 7 марта 2009.
- ↑ Helicobacter Pylori in Peptic Ulcer Disease (англ.). NIH Consensus Statement Online Jan 7–9;12(1):1-23. Проверено 4 марта 2009.
- ↑ Pietroiusti A., Luzzi I., Gomez M. J., Magrini A., Bergamaschi A., Forlini A., Galante A. (April 2005). "Helicobacter pylori duodenal colonization is a strong risk factor for the development of duodenal ulcer.". PMID 15801926.
- ↑ Ohkusa T., Okayasu I., Miwa H., Ohtaka K., Endo S., Sato N. Helicobacter pylori infection induces duodenitis and superficial duodenal ulcer in Mongolian gerbils // International Journal of Gastroenterology and Hepathology. — 2003. — № 52. — С. 797 — 803.
- ↑ The Nobel Prize in Physiology or Medicine 2005 (англ.). Nobel Foundation (2005). Проверено 5 марта 2009.
- ↑ Edgie-Mark A. Co, Neal L. Schiller Resistance Mechanisms in an In Vitro-Selected Amoxicillin-Resistant Strain of Helicobacter pylori // Antimicrobial Agents Chemotherapy. — 2006. — Т. 50. — № 12. — С. 4174 — 4176.
- ↑ Starzyñska T., Malfertheiner P. (2006). "Helicobacter and digestive malignancies.". Helicobacter 11 Suppl 1: 32 — 35. PMID 16925609.
- ↑ J.P. Euzéby Campylobacter Sebald and Véron 1963. List of Prokaryotic names with Standing in Nomenclature. Проверено 8 марта 2009.
- ↑ Vandamme P., Falsen E., Rossau R., Hoste B., Segers P., Tytgat R.,De Ley J. [http://ijs.sgmjournals.org/cgi/reprint/41/1/88 Revision of Campylobacter, Helicobacter, and Wolinella Taxonomy: Emendation of Generic Descriptions and Proposal of Arcobacter gen. nov.] // International Journal of Systematic Bacteriology. — 1991. — Т. 41. — № 1. — С. 88 — 103.
- ↑ 18,0 18,1 18,2 18,3 18,4 Volume Two, Part C: The Alpha-, Beta, Delta and Epsilonproteobacteria // Bergey's Manual of Systematic Bacteriology / Editor-in-Chief: George M. Garrity. — 2nd Edition. — New York: Springer, 2005. — Т. The Proteobacteria. — P. 1169 — 1189. — ISBN 0-387-95040-0
- ↑ Dubois A. Intracellular Helicobacter pylori and Gastric Carcinogenesis: An “Old” Frontier Worth Revisiting // Gastroenterology. — 2007. — Т. 132. — № 3. — С. 1177 — 1180.
- ↑ Olson J. W., Maier R. J. Molecular hydrogen as an energy source for Helicobacter pylori. // Science. — 2002. — Т. 298. — № 5599. — С. 1788 — 1790.
- ↑ Stark R. M., Gerwig G. J., Pitman R. S., Potts L. F., Williams N. A., Greenman J., Weinzweig I. P., Hirst T. R., Millar M. R. Biofilm formation by Helicobacter pylori. // Letters in applied microbiology. — 1999. — Т. 28. — № 2. — С. 121 — 126.
- ↑ Chan W. Y., Hui P. K., Leung K. M., Chow J., Kwok F., Ng C. S. Coccoid forms of Helicobacter pylori in the human stomach. // American Journal of Clinical Pathology. — 1994. — Т. 102. — № 4. — С. 503 — 507.
- ↑ Chaput C., Ecobichon C., Cayet N., Girardin S. E., Werts C., Guadagnini S., Prévost M.-C., Mengin-Lecreulx D., Labigne A., Boneca I. G. Role of AmiA in the Morphological Transition of Helicobacter pylori and in Immune Escape // PLoS Pathogens. — 2006. — Т. 2. — № 9. — С. e97..
- ↑ PyloriGene World-Wide Web Server (англ.). Institut Pasteur. — Геном H.pylori штаммов 26695 и J99. Проверено 4 марта 2009.
- ↑ Helicobacter pylori 26695, complete genome (англ.). NCBI. Проверено 4 марта 2009.
- ↑ Helicobacter pylori J99, complete genome (англ.). NCBI. Проверено 4 марта 2009.
- ↑ Helicobacter pylori HPAG1
- ↑ Couturier M. R., Tasca E., Montecucco C., Stein M. Interaction with CagF Is Required for Translocation of CagA into the Host via the Helicobacter pylori Type IV Secretion System // Infection and Immunity. — 2006. — Т. 74. — № 1. — С. 273 — 281.
- ↑ Reyes-Leon A., Atherton J. C., Argent R. H., Puente J. L., Torres J. Heterogeneity in the Activity of Mexican Helicobacter pylori Strains in Gastric Epithelial Cells and Its Association with Diversity in the cagA Gene // Infection and Immunity. — 2007. — Т. 75. — № 7. — С. 3445 — 3454.
- ↑ Yokoyama K., Higashi H., Ishikawa S., Fujii Y., Kondo S., Kato H., Azuma T., Wada A., Hirayama T., Aburatani H., HatakeyamaM . Functional antagonism between Helicobacter pylori CagA and vacuolating toxin VacA in control of the NFAT signaling pathway in gastric epithelial cells // Proceedings of the National Academy of Sciences of the United States of America. — 2005. — Т. 102. — № 27. — С. 9661 — 9666.
- ↑ Zambon C.-F., Navaglia F., Basso D., Rugge M., Plebani M. Helicobacter pylori babA2, cagA, and s1 vacA genes work synergistically in causing intestinal metaplasia // Journal of Clinical Pathology. — 2003. — Т. 56. — № 4. — С. 287 — 291.
- ↑ Semino-Mora C., Doi S. Q., Marty A., Simko V., Carlstedt I., Dubois A. Intracellular and Interstitial Expression of Helicobacter pylori Virulence Genes in Gastric Precancerous Intestinal Metaplasia and Adenocarcinoma // Journal of Infectious Diseases. — 2003. — Т. 187. — № 8. — С. 1165 — 1177.
- ↑ Baldwin D. N., Shepherd B., Kraemer P., Hall M. K., Sycuro L. K., Pinto-Santini D. M., Salama N. R. Identification of Helicobacter pylori Genes That Contribute to Stomach Colonization // Infection and Immunity. — 2007. — Т. 75. — № 2. — С. 1005 — 1016.
- ↑ Schweinitzer T., Mizote T., Ishikawa N., Dudnik A., Inatsu S., Schreiber S., Suerbaum S., Aizawa S.-I., Josenhans C. Functional Characterization and Mutagenesis of the Proposed Behavioral Sensor TlpD of Helicobacter pylori // Journal of Bacteriology. — 2008. — Т. 190. — № 9. — С. 3244 — 3255.
- ↑ 35,0 35,1 Nawfal R. Hussein, Marjan Mohammadi, Yeganeh Talebkhan, Masoumeh Doraghi, Darren P. Letley, Merdan K. Muhammad, Richard H. Argent, John C. Atherton Differences in Virulence Markers between Helicobacter pylori Strains from Iraq and Those from Iran: Potential Importance of Regional Differences in H. pylori-Associated Disease // Journal of Clinical Microbiology. — 2008. — Т. 46. — № 5. — С. 1774 — 1779.
- ↑ Beswick E. J., Pinchuk I. V., Minch K., Suarez G., Sierra J. C., Yamaoka Y., Reyes V. E. The Helicobacter pylori Urease B Subunit Binds to CD74 on Gastric Epithelial Cells and Induces NF-κB Activation and Interleukin-8 Production // Infection and Immunity. — 2006. — Т. 74. — № 2. — С. 1148 — 1155.
- ↑ Andrzejewska J., Lee S. K., Olbermann P., Lotzing N., Katzowitsch E., Linz B., Achtman M., Kado C. I., Suerbaum S., Josenhans C. Characterization of the Pilin Ortholog of the Helicobacter pylori Type IV cag Pathogenicity Apparatus, a Surface-Associated Protein Expressed during Infection // Journal of Bacteriology. — 2006. — Т. 188. — № 16. — С. 5865 — 5877.
- ↑ López-Vidal Y., Ponce-de-León S., Castillo-Rojas G., Barreto-Zúñiga R., Torre-Delgadillo A. High Diversity of vacA and cagA Helicobacter pylori Genotypes in Patients with and without Gastric Cancer // PLoS ONE. — 2008. — Т. 3. — № 12. — С. e3849..
- ↑ Yamazaki S., Yamakawa A., Okuda T., Ohtani M., Suto H., Ito Y., Yamazaki Y., Keida Y., Higashi H., Hatakeyama M., Azuma T. Distinct Diversity of vacA, cagA, and cagE Genes of Helicobacter pylori Associated with Peptic Ulcer in Japan // Journal of Clinical Microbiology. — 2005. — Т. 43. — № 8. — С. 3906 — 3916.
- ↑ Ivie S. E., McClain M. S., Torres V. J., Holly M. Scott Algood, Lacy D. B., Yang R., Blanke S. R., Cover T. L. Helicobacter pylori VacA Subdomain Required for Intracellular Toxin Activity and Assembly of Functional Oligomeric Complexes // Infection and Immunity. — 2008. — Т. 76. — № 7. — С. 2843 — 2851.
- ↑ Tsutsumi R., Takahashi A., Azuma T., Higashi H., Hatakeyama M. Focal Adhesion Kinase Is a Substrate and Downstream Effector of SHP-2 Complexed with Helicobacter pylori CagA // Molecular and Cellular Biology. — 2006. — Т. 26. — № 1. — С. 261 — 276.
- ↑ Ding S.-Z., Minohara Y., Fan X. J., Wang J., Reyes V. E., Patel J., Dirden-Kramer B., Boldogh I., Ernst P. B., Crowe S. E. Helicobacter pylori Infection Induces Oxidative Stress and Programmed Cell Death in Human Gastric Epithelial Cells // Infection and Immunity. — 2007. — Т. 75. — № 8. — С. 4030 — 4039.
- ↑ Методы диагностики хеликобактериоза / под ред. Козлова А. В., Новиковой В. П.. — СПб.: "Диалектика", 2008. — С. 34 — 48. — 88 с. — ISBN 978-5-98230-044-7
- ↑ Mégraud F. H. pylori antibiotic resistance: prevalence, importance, and advances in testing // International Journal of Gastroenterology and Hepathology. — 2004. — № 53. — С. 1374 — 1384.
- ↑ Holly M. Scott Algood, Timothy L. Cover Helicobacter pylori Persistence: an Overview of Interactions between H. pylori and Host Immune Defenses // Clinical Microbiology Reviews. — 2006. — Т. 19. — № 4. — С. 597 — 613.
- ↑ Kuipers E. J., Israel D. A., Kusters J. G., Gerrits M. M., Weel J., van Der Ende A., van Der Hulst R. W., Wirth H. P., Höök-Nikanne J., Thompson S. A., Blaser M. J. Quasispecies development of Helicobacter pylori observed in paired isolates obtained years apart from the same host. // Journal of infectious diseases. — 2000. — Т. 181. — № 1. — С. 273 — 282.
- ↑ Goodman K. J, O'rourke K., Day R. S., Wang C., Nurgalieva Z., Phillips C. V., Aragaki C., Campos A., de la Rosa J. M. Dynamics of Helicobacter pylori infection in a US-Mexico cohort during the first two years of life. // International Journal of Epidemiology -. — 2005. — Т. 34. — № 6. — С. 1348 — 1355.
- ↑ Goodman K., Cockburn M. The role of epidemiology in understanding the health effects of Helicobacter pylori. // Epidemiology. — 2001. — Т. 12. — № 2. — С. 266 — 271.
- ↑ Borody T. J., Cole P., Noonan S., Morgan A., Lenne J., Hyland L., Brandl S., Borody E. G., George L. L. Recurrence of duodenal ulcer and Campylobacter pylori infection after eradication. // The Medical journal of Australia. — 1989. — Т. 151. — № 8. — С. 431 — 435.
- ↑ Mirbagheri S. A., Hasibi M., Abouzari M., Rashidi A. Triple, standard quadruple and ampicillin-sulbactam-based quadruple therapies for H. pylori eradication: a comparative three-armed randomized clinical trial. // World journal of gastroenterology. — 2006. — Т. 12. — № 30. — С. 4888 — 4891.
- ↑ European Helicobacter Pylori Study Group Current Concepts in the Management of Helicobacter pylori Infection (англ.). The Maastricht 2-2000 Consensus Report. Проверено 4 марта 2009.
- ↑ Лапина Т. Л. Современное лечение язвенной болезни: новые препараты (рус.). Сателлитный симпозиум в рамках VIII Российского Национального Конгресса "Человек и Лекарство" (5 апреля 2001 г). Проверено 13 марта 2009.
- ↑ Sander J. O. Veldhuyzen van Zanten, Kolesnikow T., Leung V., Jani L. O'Rourke, Lee A. Gastric Transitional Zones, Areas where Helicobacter Treatment Fails: Results of a Treatment Trial Using the Sydney Strain Mouse Model // Antimicrobial Agents and Chemotherapy. — 2003. — Т. 47. — № 7. — С. 2249 — 2255.
- ↑ Aboderin O. A., Abdu A. R., Odetoyin B. W., Okeke I. N., Lawal O. O., Ndububa D. A., Agbakwuru A. E., Lamikanra A. Antibiotic resistance of Helicobacter pylori from patients in Ile-Ife, South-west, Nigeria // African Health Sciences. — 2007. — Т. 7. — № 3. — С. 143 — 147.
- ↑ Kato S., Fujimura S., Udagawa H., Shimizu T., Maisawa S., Ozawa K., Iinuma K. Antibiotic Resistance of Helicobacter pylori Strains in Japanese Children // Journal of Clinical Microbiology. — 2008. — Т. 40. — № 2. — С. 649 —– 653.
- ↑ Glocker E., Stueger H.-P., Kist M. Quinolone Resistance in Helicobacter pylori Isolates in Germany // Antimicrobial Agents and Chemotherapy. — 2007. — Т. 51. — № 1. — С. 346 — 349.
- ↑ Kamoda O., Anzai K., Mizoguchi J., Shiojiri M., Yanagi T., Nishino T., Kamiya S. In Vitro Activity of a Novel Antimicrobial Agent, TG44, for Treatment of Helicobacter pylori Infection // Antimicrobial Agents and Chemotherapy. — 2006. — Т. 50. — № 9. — С. 3062 — 3069.
- ↑ Dai G., Cheng N., Dong L., Muramatsu M., Xiao S., Wang M.-W., Zhu D.-X. Bactericidal and Morphological Effects of NE-2001, a Novel Synthetic Agent Directed against Helicobacter pylori // Antimicrobial Agents and Chemotherapy. — 2005. — Т. 49. — № 8. — С. 3468 — 3473.
- ↑ Raghavan S., Svennerholm A.-M., Holmgren J. Effects of Oral Vaccination and Immunomodulation by Cholera Toxin on Experimental Helicobacter pylori Infection, Reinfection, and Gastritis // Infection and Immunity. — 2002. — Т. 70. — № 8. — С. 4621 — 4627.
Ссылки[]
- Mobley, Harry L. T.; Mendz, George L.; Hazell, Stuart L. Helicobacter pylori: Physiology and Genetics. — ASM Press, 2001. — С. 626. — ISBN 1-55581-213-9
- Helicobacter pylori (англ.). MicrobeWiki. — The student-edited microbiology resource. Проверено 9 марта 2009.
| Эта статья входит в число хороших статей русского раздела Википедии. |
Эта страница использует содержимое раздела Википедии на русском языке. Оригинальная статья находится по адресу: Helicobacter pylori. Список первоначальных авторов статьи можно посмотреть в истории правок. Эта статья так же, как и статья, размещённая в Википедии, доступна на условиях CC-BY-SA .